Crean una nueva estrategia contra el cáncer que consigue mayor muerte celular con menos quimioterapia gracias a la nanomedicina
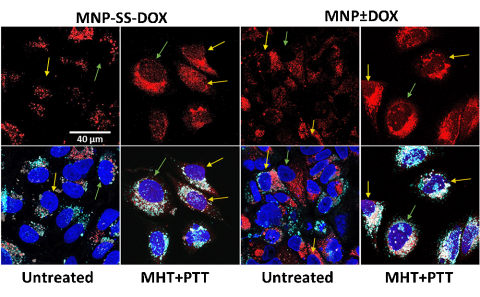
Un estudio liderado por el Instituto de Ciencia de Materiales de Madrid (ICMM-CSIC) demuestra el potencial de terapias contra el cáncer que, al combinar dos tipos de hipertermia (tratamientos con calor) con quimioterapia con nanopartículas, permiten disminuir las dosis de medicamento. El estudio, que ha sido publicado y seleccionado como portada en la revista Advanced NanoBiomed Research, avanza hacia tratamientos más efectivos y accesibles contra los tumores.
El equipo de trabajo ha creado nanopartículas magnéticas (de un tamaño que es la millonésima parte de un centímetro) a las que le ha añadido un fármaco quimioterapeútico, la doxorrubicina. Para llevar a cabo su nuevo tratamiento, llamado trimodal –porque combina tres aproximaciones sinérgicas contra el cáncer–, han realizado una estimulación magnética sobre las nanopartículas, lo que produce calor (hipertermia magnética), a la vez que han aplicado un láser en el infrarrojo cercano, que también produce calor (tratamiento fototérmico). Además, “hemos hecho que las nanopartículas liberen el fármaco justo cuando reciban este calor, lo que se conoce como quimioterapia localizada en condiciones clínicamente seguras”, explica Ana Espinosa, investigadora del CSIC en el Instituto de Ciencia de Materiales de Madrid (ICMM-CSIC) y líder del estudio.
“Al activar la liberación del fármaco sensible al pH y el calentamiento sinérgico dentro de las células cancerosas, estas nanopartículas logran una potente destrucción de células tumorales a la vez que minimizan la toxicidad sistémica”, continúa la científica.

Espinosa señala que las células cancerígenas son especialmente sensibles al calor, por lo que con este tratamiento intentan crear ‘una trampa de calor’ que acabe con esas células tumorales. “Buscamos producir un efecto terapéutico a la vez que nos permita disminuir las dosis tóxicas para los tejidos sanos”, señala la investigadora.
Como la utilización de cada técnica por separado no permite llegar de forma segura a la temperatura que se requiere, esta científica y su equipo buscaban un efecto sinérgico: “Sumas los efectos y esto te permite, además, disminuir la intensidad de los parámetros de aplicación de dosis. Podemos bajar la intensidad del láser y también el campo magnético, por lo que el tratamiento es menos agresivo”, celebra.
El estudio, que se centraba principalmente en demostrar el potencial del tratamiento trimodal, ha trabajado con nanopartículas magnéticas de óxido de hierro porque esta sustancia se absorbe bien en el organismo, se degrada de manera natural y, en estas dosis, no es tóxico.
“Hemos conseguido una muerte celular que es hasta un 70% más eficiente que con las terapias individuales”, detalla Espinosa. Los estudios, de momento, se han realizado en modelos in vitro de células tumorales de cáncer de mama, aunque podrían extenderse a cualquier tipo de cáncer y son replicables a mayor escala.
Los hallazgos “resaltan la posible aplicación clínica de los sistemas de nanopartículas multifuncionales para terapias contra el cáncer específicas y de baja toxicidad, avanzando hacia tratamientos más efectivos y accesibles”, concluye la investigadora.
El trabajo es una colaboración entre el Instituto de Ciencia de Materiales de Madrid (ICMM-CSIC), el Instituto IMDEA Nanociencia, el Instituto Curie (Francia) y el Instituto de Cerámica y Vidrio (ICV-CSIC).
Referencia Bibliográfica:
Rosalía López-Méndez, Nuria Lafuente-Gómez, Eva Céspedes, Mónica Dhanjani, Marina París-Ogáyar, Francisco José Terán, Aida Serrano, Julio Camarero, Gorka Salas, Claire Wilhelm, Álvaro Somoza, Ana Espinosa*. Tri-Modal Anticancer Strategies with Doxorubicin-Loaded Iron Oxide Nanoparticles Integrating Chemo and Magneto-Photothermal Therapeutic Effects. Advanced NanoBiomed Research. DOI: https://doi.org/10.1002/anbr.70084
ICMM
Sor Juana Ines de la Cruz, 3
Cantoblanco, 28049
Madrid, España
Teléfono: (+34) 91 334 90 00
Email: @email
Oficina de Comunicación/Prensa: @email

Acknowledge the Severo Ochoa Centres of Excellence program through Grant CEX2024-001445-S/ financiado por MICIU/AEI / 10.13039/501100011033

Contacto | Accesibilidad | Aviso legal | Política de Cookies | Protección de datos
